Radiotividade
A radioatividade é definida como a capacidade que alguns elementos fisicamente instáveis possuem de emitir energia sob forma de partículas ou radiação eletromagnética.
A radioatividade foi descoberta no século XIX. Até esse momento predominava a ideia de que os átomos eram as menores partículas da matéria. Com a descoberta da radiação, os cientistas constataram a existência de partículas ainda menores que o átomo, tais como: próton, nêutron, elétron. Vamos rever um pouco dessa história?
- No ano de 1896, o físico francês Antoine-Henri Becquerel (1852-1908) observou que um sal de urânio possuía a capacidade de sensibilizar um filme fotográfico, recoberto por uma fina lâmina de metal.
- Em 1897, a cientista polonesa Marie Sklodowska Curie (1867-1934) provou que a intensidade da radiação é sempre proporcional à quantidade do urânio empregado na amostra, concluindo que a radioatividade era um fenômeno atômico.
Anos se passaram e a ciência foi evoluindo até ser possível produzir a radioatividade em laboratório. Veja a diferença entre radiação natural e artificial:
• Radioatividade natural ou espontânea: é a que se manifesta nos elementos radioativos e nos isótopos que se encontram na natureza.
• Radioatividade artificial ou induzida: é aquela produzida por transformações nucleares artificiais.
A radioatividade geralmente provém de isótopos como urânio-235, césio-137, cobalto-60, tório-232, que são fisicamente instáveis e radioativos, possuindo uma constante e lenta desintegração. Tais isótopos liberam energia através de ondas eletromagnéticas (raio gama) ou partículas subatômicas em alta velocidade: é o que chamamos de radiação. O contato da radiação com seres vivos não é o que podemos chamar de uma boa relação.
Os efeitos da radiação podem ser em longo prazo, curto prazo ou apresentar problemas aos descendentes da pessoa infectada (filhos, netos). O indivíduo que recebe a radiação sofre alteração genética, que pode ser transmitida na gestação. Os raios afetam os átomos que estão presentes nas células, provocando alterações em sua estrutura. O resultado? Graves problemas de saúde como a perda das propriedades características dos músculos e da capacidade de efetuar as sínteses necessárias à sobrevivência.
A radioatividade pode apresentar benefícios ao homem e por isso é utilizada em diferentes áreas. Na medicina, ela é empregada no tratamento de tumores cancerígenos; na indústria é utilizada para obter energia nuclear; e na ciência tem a finalidade de promover o estudo da organização atômica e molecular de outros elementos.
Emissão alfa (α)
A radiação alfa é positiva, sendo constituída de dois prótons e dois nêutrons. Seu poder de penetração é baixo, causando pequenos danos ao ser humano.
As principais emissões radioativas são a alfa (α), a beta (β) e a gama (γ). Nesse artigo, falaremos sobre a primeira dessas três radiações, como se deu sua descoberta, do que ela é constituída, como a sua radiação afeta a estrutura da matéria, qual o seu poder de penetração e quais são os danos que causa ao ser humano.
Em 1900, independentemente e quase ao mesmo tempo, o físico neozelandês Ernest Rutherford (1871-1937) e o químico francês Pierre Curie (1859-1906) conseguiram identificar experimentalmente as partículas alfa e beta.
Rutherford realizou um experimento que ficou famoso, no qual ele montou uma aparelhagem semelhante à mostrada na ilustração abaixo:
Rutherford realizou um experimento que ficou famoso, no qual ele montou uma aparelhagem semelhante à mostrada na ilustração abaixo:
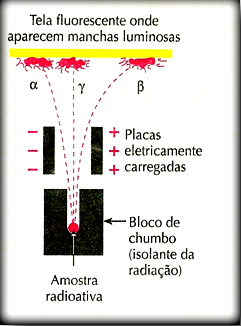
Ele colocou uma amostra de um elemento radioativo em um bloco de chumbo com um orifício. Visto que o chumbo bloqueia as emissões radioativas, elas não se espalhariam pelo ambiente, mas seriam orientadas a sair na direção da única abertura no chumbo. Esse aparelho foi colocado dentro de um recipiente submetido ao vácuo. A esse aparelho foram adaptadas duas placas eletrizadas com cargas opostas – isto é, aplicou-se um potencial elétrico. Na parede oposta ao bloco de chumbo foi colocada uma chapa fotográfica ou uma tela com sulfeto de zinco, material fluorescente, que registraria as emissões radioativas.
Um dos fatores observados com esse experimento foi que o percurso da radiação alfa foi desviado para o polo negativo da placa. Conforme é de conhecimento geral, cargas opostas se atraem, consequentemente, concluiu-se que as radiações alfa são, na realidade, partículas positivas.
- Constituição:
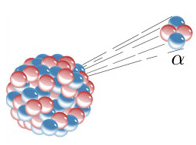
Com o tempo, descobriu-se que essas partículas positivas são, na verdade, formadas por dois prótons e dois nêutrons (42α2+), isto é, iguais a um núcleo de hélio (42He). Além disso, são partículas pesadas, de massa elevada, pois sofreram desvio pelo campo eletromagnético.
- Consequências da emissão de partículas alfa para a estrutura do átomo:
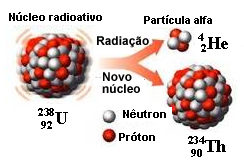
Conforme sabemos, a emissão de radiação é um processo que acontece a partir do núcleo – daí o termo reações nucleares. Portanto, envolve uma variação da carga nuclear (positiva), causando alterações na substância.
No caso da emissão de uma partícula alfa (42α2+), o número atômico (quantidade de prótons) do átomo diminui duas unidades (porque perdeu dois prótons) e seu número de massa (quantidade de prótons e nêutrons no núcleo) diminui quatro unidades.
Veja como isso ocorre na emissão de uma partícula alfa de um átomo de um elemento genérico (ZAX):
ZAX → 42α2+ + Z-2A-4X
Exemplo:
92238U → 42α2+ + 90234Th
A radiação alfa também tem um poder de ionização alto, podendo capturar dois elétrons e se tornar um átomo de hélio:
42α2+ + 2 e- → 42He
- Poder de penetração:
A velocidade das partículas alfa é baixa, sendo inicialmente de 3 000 km/s até 30 000 km/s. A sua velocidade média é de aproximadamente 20 000 km/s, que é 5% da velocidade da luz. Por ser lenta, a radiação alfa tem um poder de penetração muito baixo, não atravessando nem mesmo uma folha de papel, roupas ou pele.
Veja na figura abaixo a comparação do seu poder de penetração com as outras emissões beta e gama:
.jpg)
- Danos causados ao ser humano:
Em razão do seu baixo poder de penetração, os danos que as partículas alfa causam ao ser humano são pequenos. Quando incidem sobre o nosso corpo, elas são detidas pela camada de células mortas da pele, podendo, no máximo, causar queimaduras.
Emissão beta (β)
As emissões beta são formadas por elétrons emitidos com alta velocidade e, portanto, com alta energia, pelos núcleos.
O químico neozelandês Ernest Rutherford realizou um experimento no qual colocou uma amostra de um material radioativo em um bloco de chumbo, com um furo para direcionar as emissões radioativas; e submeteu essas radiações a um campo eletromagnético.
Dentre os resultados obtidos, Rutherford percebeu que um feixe de radiações era atraído pela placa positiva, o que o levou a concluir que essas emissões eram decarga negativa. Essa radiação ficou sendo chamada de raios ou emissões beta (β).
Visto que os raios sofriam deflexão quando submetidos a um campo eletromagnético, isso o levou a concluir também que eles eram na verdade compostos por partículas que apresentam massa. A massa dessas partículas, porém, era menor que a das partículas que constituíam as emissões alfa, porque as partículas β sofriam maior desvio.
- Constituição:
Em 1900, o físico francês Antoine-Henri Bequerel (1852-1908) comparou esses desvios sofridos pelas partículas beta com os desvios que os elétrons realizavam, quando também eram submetidos a um campo eletromagnético. O resultado foi que eram iguais; com isso, viu-se que as partículas beta eram na realidade elétrons.
Em razão disso, a representação dessa partícula é dada por 0-1β ou β-. Veja que a emissão beta apresenta número de massa (A) igual a zero, pois os elétrons não fazem parte do núcleo do átomo.
- Consequências da emissão de partículas beta para a estrutura do átomo:
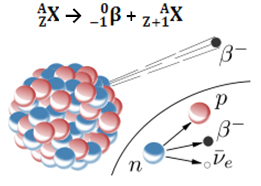
A emissão de uma partícula beta (0-1β) é resultado do rearranjo do núcleo instável do átomo radioativo de modo a adquirir estabilidade. Para tanto, ocorre um fenômeno no núcleo, no qual um nêutron se decompõe originando três novas partículas: um próton, um elétron (partícula β) e um neutrino. O antineutrino e o elétron são emitidos; o próton, no entanto, permanece no núcleo.
10n →11p + 0-1e + 00ν
nêutron próton elétron neutrino
Dessa forma, quando um átomo emite uma partícula beta, ele se transforma em um novo elemento com o mesmo número de massa (porque o nêutron que havia antes foi “substituído” pelo próton), mas o seu número atômico (Z = prótons no núcleo) aumenta uma unidade.
Veja a seguir como isso ocorre de modo genérico:
Veja um exemplo de decaimento beta que ocorre com o isótopo 14 do elemento carbono:
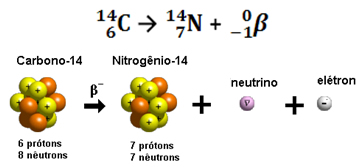
A radiação beta é constituída de elétrons emitidos à grande velocidade pelos núcleos dos átomos radioativos, sendo que essa velocidade inicial é de 100 000 km/s até 290 000 km/s e chegam a atingir 95% da velocidade da luz.
A massa da radiação β é a mesma de um elétron, que é 1840 vezes menor que a de um próton ou de um nêutron. A radiação alfa (α) emite dois prótons e dois nêutrons, assim a massa das partículas α é 7360 vezes maior que a das partículas β. Isso explica o fato de as partículas α sofrerem um desvio menor que as partículas β, conforme Rutherford havia verificado em seu experimento.
- Poder de penetração:
Seu poder de penetração é médio, sendo de 50 a 100 vezes mais penetrante que as partículas alfa. Estas podem atravessar uma folha de papel, mas são detidas por uma chapa de chumbo de apenas 2 mm ou de alumínio de 2 cm. Quando incidem no corpo humano, podem penetrar até 2 cm.
- Danos causados ao ser humano:
Visto que seu poder de penetração sobre o corpo humano é de apenas 2 cm, as partículas β podem penetrar na pele, causando queimaduras, mas são barradas antes de atingir órgãos mais internos do corpo.
Emissões gama
As radiações gama são ondas eletromagnéticas com alto poder de penetração, podendo atravessar o corpo humano e causar vários danos.
No texto “Emissões alfa (α)” foi citado um experimento realizado por Rutherford, que consistiu basicamente em colocar uma amostra de material radioativo em um bloco de chumbo. Por meio de um furo no bloco e de um campo eletromagnético, orientaram-se as emissões radioativas.
O físico francês Paul Ulrich Villard (1860-1934) repetiu esse experimento – no mesmo ano em que Rutherford o realizou (1900) – e verificou que uma das radiações emitidas não sofria desvio pelo campo eletromagnético. Isso significa que essas emissões não eram constituídas de partículas, como as radiações alfa (α) e beta (β), mas eram, na verdade, radiações eletromagnéticas.
.jpg)
Essa radiação eletromagnética emitida pelos elementos radioativos foi denominada radiação gama e representada pela letra grega γ.
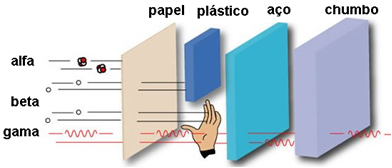
Elas são semelhantes aos raios X, não possuindo carga elétrica e nem massa. Porém, são mais energéticas que os raios X, porque seu comprimento de onda é bem menor, ficando entre 0,1 Å e 0,001Å. Elas são capazes de atravessar milhares de metros no ar, folhas de papel, placas de madeira, 15 cm de aço e somente são detidas por placas de chumbo ou por mais de 5 cm de paredes grossas de concreto.
Além disso, seu alto poder de penetração também se deve ao fato de que, como não possui carga elétrica, não sofre interferência dos elétrons e prótons dos átomos dos materiais que atravessa.
Em razão disso, as emissões gama podem atravessar um corpo humano e causar danos irreparáveis. Quando passa através da matéria, essa radiação interage com as moléculas, resultando em íons e radicais livres, sendo que esses últimos são prejudiciais às células vivas. Algumas células se mostram mais sensíveis, como as do tecido linfático, as da medula, as das membranas mucosas intestinais, as das gônadas e as do cristalino dos olhos.
Veja a seguir o seu poder de penetração em comparação às radiações alfa e beta:
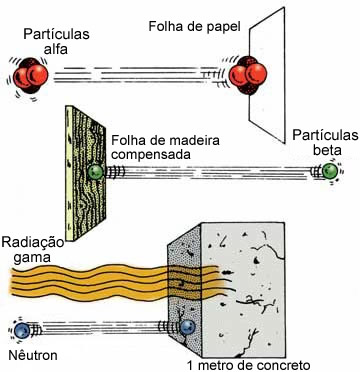
Elas são emitidas pelo núcleo imediatamente após a saída das partículas α ou β. Por isso, mesmo um elemento emissor de partículas alfa pode ser perigoso, pois também emite raios γ.
Descoberta dos Pósitrons
Os pósitrons são partículas que possuem carga positiva e massa próximas às do elétron e que foram descobertas por Irene Curie e seu marido, Frederic Joliot.
O método diagnóstico de cintilografia óssea é feito com emissão de pósitrons
Irene Curie (1897-1956), filha de Marie Curie, e seu marido Frederic Joliot (1900-1958) realizaram, no ano de 1934, experimentos de transmutação artificial, no quais bombardearam o alumínio 1327Al com partículas alfa (24α) e conseguiram obter um isótopo do fósforo (1530P) e um nêutron.
1327Al + 24α → 1530P + 01n
O mais interessante, porém, foi que eles observaram que esse isótopo do fósforo era radioativo e que ele emitia uma partícula com massa igual à do elétron; no entanto, a sua carga era positiva. Eles viram também que, quando o bombardeamento de partículas alfa era interrompido, o alumínio deixava de emitir nêutrons, mas continuava a lançar pósitrons, do mesmo modo que as partículas alfa e beta são emitidas na radioatividade natural – indicando que realmente os pósitrons eram emitidos pelo fósforo e não pelo alumínio.
A essa nova partícula radioativa foi dado o nome de pósitron, ou partícula beta positiva, sendo representada por +10e ou β+, ou, ainda, +10β. Hoje se sabe que o pósitron é, na verdade, uma antipartícula beta negativa.
A reação nuclear desse processo estudado por Irene e Frederic é representada por:
1530P → +10e + 1430Si
Observe que quando o radioisótopo, que no caso é o fósforo, emite um pósitron, seu número atômico (Z = prótons) diminui uma unidade e seu número de massa (A = prótons + nêutrons) permanece inalterado. Veja mais dois exemplos:
815O→ +10e + 715O (Note que 15 = 0 + 15 e 8 = 1 + 7)
611C → +10e + 511B (Note que 11 = 0 + 11 e 6 = 1 + 5)
Os pósitrons são emitidos por radioisótopos que possuem elevado número de prótons.
A emissão de pósitrons é usada na medicina em diagnósticos por imagem cintilográfica, conhecida comopósitron emission tomografia (PET). Esse método diagnóstico estuda a medula óssea por meio da injeção do marcador radioativo e é útil principalmente na avaliação de processos inflamatório/infecciosos (osteomielite aguda). Esse marcador radioativo tem a capacidade de se agregar à matriz óssea proporcionalmente ao fluxo sanguíneo na região e à atividade metabólica. Com isso, realiza-se uma fotografia do corpo ou algumas imagens localizadas, quando há indicação.

Meia-Vida
A meia-vida de um elemento radioativo consiste no tempo em que uma amostra desse elemento leva para reduzir-se à metade.

A meia-vida é um fenômeno nuclear e, por isso, não é influenciada por fatores externos, como a quantidade de massa inicial ou a variação da pressão e temperatura.

Tomando como exemplo 16g de massa do isótopo radioativo 1532P, teremos o seguinte gráfico:
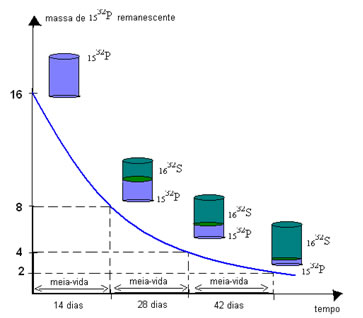
Conforme o gráfico, o período de meia-vida do 1532Pé de 14 dias, pois exatamente neste tempo ele é reduzido pela metade, ou seja, de 16 g para 8 g, originando o1632S.
Pode-se, além da massa, relacionar também o número de átomos para a relação da meia-vida.
Leis da Radiotividade
As leis da radioatividade se referem às alterações que ocorrem no núcleo do átomo quando se emitem partículas alfa (α) ou beta (β).
Primeira Lei: Lei de Soddy
O físico-químico inglês Frederick Soddy (1877-1956) foi um pioneiro no estudo da radioatividade. Ele verificou que o decaimento radioativo ocorre sempre de acordo com algumas leis básicas. Dentre elas, a primeira lei da radioatividade, conhecida comoP rimeira Lei de Soddy, ou simplesmente Lei de Soddy, refere-se ao decaimento radioativo pela emissão de uma partícula alfa.
Segundo essa lei, quando um átomo de um elemento emite uma partícula alfa – que é constituída de dois prótons e dois nêutrons (42α+2) – ele se transforma em outro elemento químico. Isso ocorre porque seu número atômico (Z = prótons no núcleo) diminui duas unidades e seu número de massa (A = prótons + nêutron) diminui quatro unidades.
Isso pode ser visualizado no decaimento genérico abaixo:
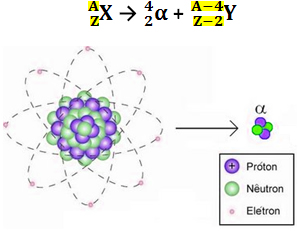
Isso significa que o átomo Y estará sempre localizado duas casas à esquerda de X na Tabela Periódica.
Veja alguns exemplos de como isso ocorre na prática:
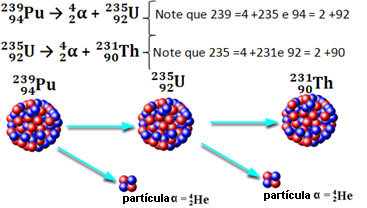
Segunda Lei: Lei de Soddy, Fajans, Russel
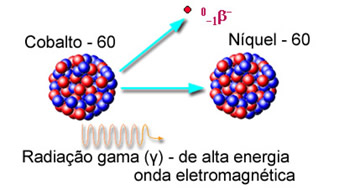
90Th234 → -1β0 + 91Pa234
Exemplo:
Dada a equação:
90X204 → xα + yβ + 92Y192
Determinar x e y
Resolução:
90X204 → x+2α4 + y-1β0 + 92Y192
Montamos duas equações:
a) uma para os índices superiores:
204 = 4x + 0y + 192
x = 3
b) uma para os índices inferiores:
90 = 2x + (-1y) + 92
90 = 2(3) -1y +92
y = 8
90X204 → 3+2α4 + 8-1β0 + 92Y192
EFEITOS DA RADIOATIVIDADE NOS ORGANISMOS
Os efeitos da radioatividade no ser humano dependem da quantidade acumulada no organismo e do tipo de radiação. A radioatividade é inofensiva para a vida humana em pequenas doses, mas, se a dose for excessiva, pode provocar lesões no sistema nervoso, no aparelho gastrintestinal, na medula óssea, etc., Muitas vezes pode levar a morte (em poucos dias ou num espaço de dez a quarenta anos, através de leucemia ou outro tipo de câncer).
Estar em contato com a radiação é algo sutil e impossível de ser percebido imediatamente, já que no momento do impacto não ocorre dor ou lesão visível.
A radiação ataca as células do corpo, fazendo com que os átomos que compõem as células sofram alterações em sua estrutura. As ligações químicas podem ser alteradas, afetando o funcionamento das células. Isso provoca, com o tempo, conseqüências biológicas no funcionamento do organismo como um todo; algumas conseqüências podem ser percebidas a curto prazo, outras a longo prazo. Às vezes vão apresentar problemas somente os descendentes (filhos, netos) da pessoa que sofreu alguma alteração genética induzida pela radioatividade.

